A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou a Fundação Hemocentro de Ribeirão Preto (FUNDHERP), em parceria com o Instituto Butantan, a iniciar um ensaio clínico no Brasil com medicamento especial à base de células geneticamente modificadas, as chamadas "células CAR-T".
De acordo com a agência, os estudos estão em fase clínica inicial. O objetivo é avaliar a segurança e a eficácia no tratamento de pacientes com leucemia linfoide aguda B e linfoma não Hodgkin B, recidivados e refratários (ou seja, em casos de reaparecimento da doença ou de resistência ao tratamento padrão).
O tratamento inovador envolve biotecnologia avançada. Os pesquisadores brasileiros promovem a reprogramação das próprias células do paciente para atacar e destruir o câncer de forma precisa. Em laboratório, é feita a transferência de genes de interesse para as células de defesa (linfócito T) do paciente.
"A aprovação desse ensaio clínico é parte de um projeto inovador de colaboração regulatória entre a Anvisa e pesquisadores e desenvolvedores brasileiros. O objetivo é impulsionar o desenvolvimento de produtos de terapias avançadas disponíveis no Sistema Único de Saúde (SUS).", diz a Anvisa.
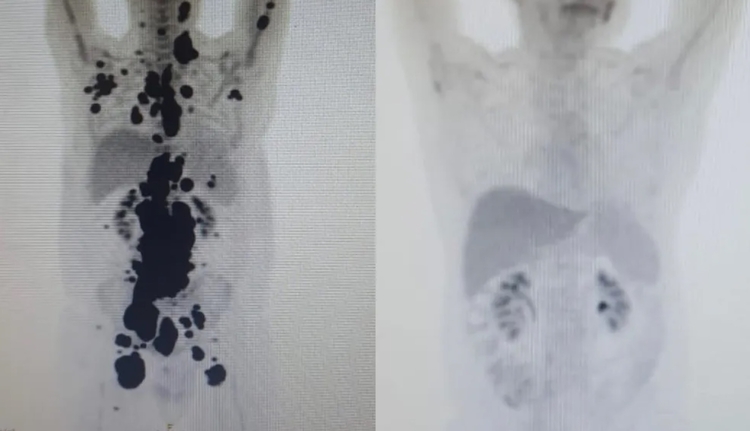
Paciente teve remissão completa - Com verbas da Fundação de Amparo à Pesquisa do Estado de São Paulo (Fapesp) e do Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq), 14 pacientes foram tratados com o CAR-T Cell e todos tiveram remissão de ao menos 60% dos tumores.
Paulo Peregrino, de 61 anos, estava há 13 anos lutando contra o câncer e teve remissão completa após um mês de tratamento. Ele estava prestes a receber cuidados paliativos quando foi selecionado para o teste.